Oddělování složek směsi
Oddělování složek směsi
V minulém článku jsme si řekli, že se látky mohou skládat z více, než jedné složky. Jak tyto složky můžeme od sebe oddělit se dozvíte v tomto článku.
1. Usazování (sedimentace)
Pro sedimentaci se můžeme rozhodnout, máte li od sebe oddělit složky suspenze (pevná látka + kapalina) nebo emulze (kapalina + kapalina). Funguje velice jednoduše a to na principu rozdílných hustot dvou látek - látka s vyšší hustotou se usadí na dně. Sedimentaci lze urychlit v tzv. odstředivce (centrifuga), kde dojde k urychlení sedimentace vlivem odstředivé síly.
Sedimentace krve se využívá ve zdravotnictví coby běžbé vyšetření. Využívá toho, že se červené krvinky shlukují do větších celků, které se pak usazují.

Sedimentace sěsi vody a oleje
(voda je pro přehlednost obarvena síranem měďnatým)
2. Krystalizace
Pomocí krystalizace oddělujeme vevnou látku z kapaliny, přičemž pevná látka je v kapalině rozpuštěná.(Například roztok kuchyňské soli ve vodě).
Abychom plně pochopili princip, musíme si něco říct k nasycenosti roztoků. Z tohoto hlediska dělíme roztoky na
- nenasycený roztok: jedná se o roztok látky v rozpouštědle za daných podmínek, kdy jsme schopni ještě v rozpouštědle dále rozpustit další množství látky, aniž bychom museli pozměnit původní podmínky (například záhřát roztok)
- nasycený roztok: jedná se o roztok, který už obsahuje maximální množství látky, které bylo možno v rozpouštědle rozpustit za daných podmínek - po přidání dalšího množství látky do tohoto roztoku už nedojde k jejímu rozpuštění (pokud nezměníme podmínky - např. zahřátím)
- přesycený roztok: je roztok, ve kterém rozpouštědlo rozpustilo maximální množství látky, jaké může rozpustit (tzn. vznikne nasycený roztok), avšak v roztoku nám zůstalo nějaké nerozpuštěné množství látky. V podstatě se tak jedná o suspenzi (pevná látka v kapalině).
A nyní zpět ke krystalizaci. Krystalizace funguje na principu, že se rozpouštědlo pomalu odpařuje, čímž roste koncentrace látky v roztoku, a to až do doby, než je roztok nasycený (odpařila se část rozpouštědla a zbylá část rozpouštědla může rozpustit už jen právě takové množství látky, které je rozpuštěno v roztoku). Nicméně rozpouštědlo se odpařuje dál, a tak nám vzniká roztok přesycený a krystalky látky se nám začínají vylučovat.
Pakliže jste princip ani teď nepochopili, pokusím se to vysvětlit na příkladu:
Máme 20 g pevné látky a 100 ml rozpouštědla. 100 ml rozpouštědla je schopno rozpustit 40 g dané látky. Vytvoříme-li roztok 20 g této látky ve 100 ml rozpouštědla, máme roztok nenasycený (rozpouštědlo rozpustí 40 g, ale my jsme použili pouze 20 g). Nyní necháme rozpouštědlo odpařovat. Jakmile nám zbyde 50 ml rozpouštědla (50 ml se odpaří), vzniká nám roztok nasycený (100 ml rozpustí 40 g, 50 ml tedy rozpustí 20 g, což je množství, které jsme na začátku rozpustili). A konečnou fází je, když se rozpouštědlo odpařuje dál, čímž vznikne přesycený roztok.
Rušená krystalizace: Funguje na principu, že přesyceného roztoku dosáhneme ochlazením daného roztoku. Rozpouštědla rozpouštějí s rostoucí teplotou větší množství látek, máme-li tedy za určité teploty nasycený roztok, pak dojde při ochlazení tohoto roztoku ke krystalizaci (roztok s nižší teplotou má nižší schopnost rozpouštět látky - není schopen rozpustit takové nožství látky, jaké při zahřátí).
3. Filtrace
Filtrace slouží k oddělení suspenzí - pevných látek rozptýlených v kapalině. Tuto směs nalijeme do nálevky s vloženým filtračním papírem - na filtračním papíru se nám zachytávají pevná část složky a dolů nám prokapává kapalina.
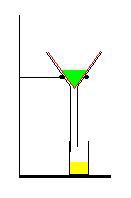
Na obrázku vidíte filtrační aparaturu - ve stojanu je umístěn filtrační kruh, který drží nálevku. V nálevce je vložený viltrační papír, který právě filtruje směs (zelené pole). Pod nálevkou se nachází kádinka, ve které je filtrát (žluté pole).
4. Sublimace
Sublimaci můžeme použít tam, kde máme oddělit od sebe dvě pevné složky, z nichž jedna sublimuje. Sublimovanou látku pak necháme ochladit (desublimovat).
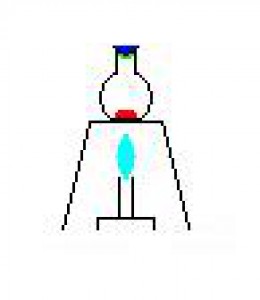
Na obrázku vidíte sublimační aparaturu. Jedná se o kahan, nad kterým je umístěna laboratorní trojnožka s azbestovou síťkou. Na síťce je položená baňka s rovným dnem, v níž je sublimovaná směs a jejíž hrdlo je přikryto hodinovým sklíčkem, ve kterém je voda (ochlazovací médium). Na spodní straně hodinového skla se desublimují krystalky sublimované látky.Místo hodinového skla jde použít laboratorní baňku s kulatým dnem naplněnou vodou.
5. Chromatografie
Chromatografiie je oddělování složek směsi fungující na proncipu rozdílné distribuci různých složek mezi pohyblivou a pevnou fází.
Pro pochopení lze uvést jednoduchý příklad, a to oddělení barviv listu. List obsahuje různá barviva. Pakliže chceme zjistit jaká, naneseme vzorek těchto barviv (vzorek směsi) na pevnou (stacionární) fázi, což může být křída, filtrační papír nebo Silufol. Tuto pevnou fází pak dáme do pohyblivé féze (což je nějaké rozpouštědlo nejčastěji ethanol, methanol...) tak, aby nanesený vzorek na pevné fázi nebyl ponořen. Pevná fáze nyní bude nasávat rozpouštědlo (pohyblivou fázi), které dojde až k nanesenému vzorku a začne jej unášet směrem vzhůru. Různé části směsi se však různě distribuují, takže některé zůstanou v nižších sférách stacionární fáze, jiné ve vyšších.
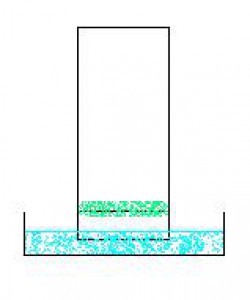

Zleva: Schématický obraz chromatografie, stacionární fáze s naneseným barvivem z listu a stacionární fáze se vzorkem z lihového fixu (oboje stacionární fáze jsou proužky filtračního papíru)
Popis schématického zobrazení chromatografie: Ve spodní části se nachází Petriho miska s rozpouštědlem (pohyblivá fáze) do níž je ponořena pevná fáze s nanezeným vzorkem směsi.


Pevné fáze se vzorky po chromatografii. Zleva: chromatografie barviva z listu, chromatografie barviva z lihového fixu, jiná chromatografie téhož vzorku směsi, jako na prvním obrázku. Ve všech případech byly jako pevné fáze použity proužky filtračního papíru a jako pohyblivá fáze líh (ethanol).
Na chromatografii chlorofylu v praxi se můžete podívat zde.
6. Destilace
Destilace je oddělování dvou a více kapalin od sebe, kdy se kapaliny v sobě mísí. Funguje na rozdílných bodech varu těchto kapalin, kdy kapalinu s nižším bodem varu necháme vyvařit a páry v chladiči opět kondenzují na kapalinu. Tímto způsobem se zpracovává ropa na využitelné látky (benzín, nafta, petrolej...) nebo kvas na alkohol.
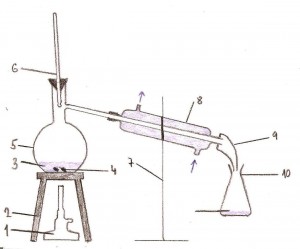
Na obrázku vidíte schématický nákres destilační aparatury, kde 1. kahan, 2. trojnožka s azbestovou síťkou, 3. směs dvou mísitelných kapalin, 4. varné kamínky, 5. destilační baňka, 6. teploměr, 7. stojan na chladič, 8. vodní přímý chladič, 9. alonž, 10. Erlenmeyerova baňka, 11. destilát
Princip: Kahanem zahřívame směs do doby, než nedosáhneme bodu varu jedné z kapalin. Tato kapalina se začíná vypařovat, páry směřují přes boční vývod baňky do chladiče, ktrým protéká voda. V chladiči páry kondenzují a skrze alonž vytéká destilát do Erlenmeyerovy baňky.
Varné kamínky jsou v baňce proto, aby nedošlo k utajenému varu, což je přehřátí kapaliny nad její bod varu a k náhlému prudkému varu (čímž by se směs mohla dostat až k bočnímu vývodu baňky a dále, čímž by znečistila destilát.